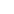西安交大科研人员在新型益生菌复合体靶向协同治疗结肠炎方面取得重要进展
- 发布时间:
- 2024-10-13
- 文章标题:
- 西安交大科研人员在新型益生菌复合体靶向协同治疗结肠炎方面取得重要进展
- 内容:
结肠炎(UC)是一种慢性、复发性的肠道粘膜损伤,主要表现为肠粘液层耗竭、紧密连接异常和肠屏障功能障碍。肠粘液层和紧密连接是密不可分的。当二者受损时,病原菌和毒素入侵损伤肠上皮并引发炎症反馈循环,从而使UC逐渐恶化。目前,口服微生态制剂调控肠道内稳态在治疗肠道疾病方面展现出较大应用前景。然而,益生菌无法有效修复肠粘膜屏障并终止炎症反馈循环,使其疗效受到限制。此外,口服益生菌受到胃肠道内的恶劣环境(强酸、消化酶和氧化应激等)影响;益生菌肠道内定殖不足、无法靶向投递到肠炎部位;肠道病理环境中匮乏的营养支持等因素的限制,而益生菌消耗粘蛋白(MUC)会造成肠道损伤。这些情况严重阻碍了口服微生态制剂在肠道疾病上的应用。因此,研制新型益生菌复合体使其能够克服上述不足成为临床的迫切需要。
图1. 胃肠道自适应和营养自供的Akkermansia muciniphila-明胶多孔微凝胶作为“创可贴”靶向协同治疗肠炎
针对以上问题,西安交通大学第一附属医院佘军军教授/王雅副研究员/生命学院吴道澄教授团队提出了一种精准覆盖肠道炎症部位来修复肠粘膜屏障和打破炎症反馈循环来协同治疗UC的策略(图1)。设计、制备了胃肠道自适应和营养自供的益生菌Akkermansia muciniphila (AKK)-明胶多孔微凝胶(AKK@GPMGs)作为精准覆盖炎症部位的“创可贴”,不仅可以抵抗胃肠道内的恶劣环境,还能够肠道在炎症部位精准释放AKK@PMP协同治疗UC,由于其自身携带粘蛋白(MUC)而不消耗肠粘蛋白,取得了显著的综合疗效。
该策略利用天然多酚原花青素(PAs)与Ca2+、肠粘液层的主要成分粘蛋白(MUC)和维持粘液层疏水性的磷脂酰胆碱(PC)在益生菌AKK表面逐层包裹,制备了具有营养自供、抗炎和抗氧化能力的益生菌复合物(AKK@PAs-MUC-PC,AKK@PMP)。随后,将AKK@PMP封装在明胶多孔微凝胶中制备出“遇酸封闭”和“遇酶释放”的AKK@GPMGs。AKK@GPMG表面的氢键在胃酸环境中破坏,导致官能团质子化,从而胶原蛋白肽链分散封闭孔洞,充当屏障保护内部AKK@PMP;AKK@GPMGs分子结构中的多肽序列可被肠炎部位的基质金属蛋白酶(MMP)特异性识别和分解,靶向释放AKK@PMP;AKK@PMP类似“创可贴”一样紧密覆盖于发炎肠道部位,促进AKK和PAs-MUC-PC持久协同作用。此外,PAs-MUC-PC层中的MUC-PC可为AKK提供营养并创造适宜的生长环境,避免了对肠粘膜的额外消耗。最终,AKK@GPMGs的每种组分协同作用,实现了对肠炎增强的精准靶向协同治疗。
该工作以《胃肠道自适应和营养自供的Akkermansia muciniphila-明胶多孔微凝胶协同治疗UC》(“Gastrointestinal Self-Adaptive and Nutrient Self-Sufficient Akkermansia muciniphila-Gelatin Porous Microgels for Synergistic Therapy of Ulcerative Colitis”)为题在著名期刊《美国化学会·纳米》(ACS Nano, IF=15.8)上在线发表。文章第一作者为西安交通大学第一附属医院博士生张玉杰,西安交通大学第一附属医院为该论文的第一和通讯作者单位,佘军军教授、王雅副研究员和吴道澄教授为通讯作者。该研究成果是佘军军教授课题组在肠道疾病治疗领域的又一重要进展。
该工作得到了国家自然科学基金、国家博士后创新人才计划、博士后科学基金、陕西省自然科学基础研究计划等的资助。西安交通大学分析测试中心和生物医学实验中心为本工作提供了大量研究支持。
论文链接:https://doi.org/10.1021/acsnano.4c07658